Der spannende Fall
Kooperation Illumina und Münchner Leukämielabor
Hintergrund
Im Rahmen unseres großen Forschungsprojektes haben wir in den letzten drei Jahren mehr als 5.500 Fälle mit WGS und WTS in unserem Labor analysiert und diese für viele wissenschaftliche Projekte ausgewertet. Gleichzeitig haben wir an einer bioinformatischen Pipeline gearbeitet, die es uns erlaubt, unsere klassischen Befunde aus Zytogenetik, FISH und Molekulargenetik (zumeist Gen-Panels) als so genannte „orthogonale“ Daten mit den Daten des WGS und WTS zu vergleichen. Damit können wir die Vor- und Nachteile der aktuellen Goldstandard-Diagnostik im Vergleich zu einer potentiell zukünftigen, genombasierten Diagnostik erarbeiten.
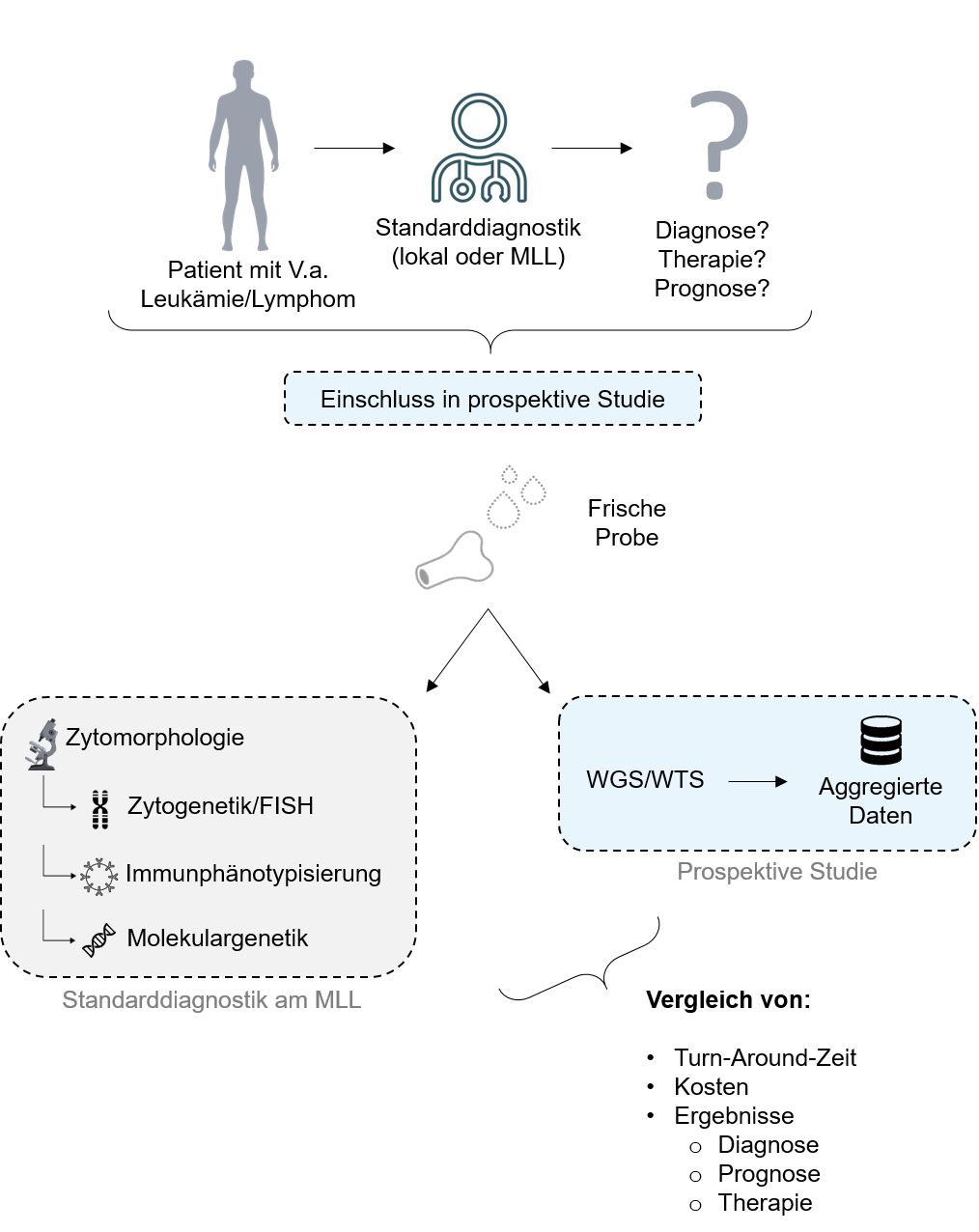
Jetzt möchten wir gern prospektiv prüfen, ob WGS & WTS zusätzliche Erkenntnisse bei Patienten erbringen kann, bei denen die aktuelle Standard-Diagnostik Fragen offen ließ. Im Detail möchten wir evaluieren:
- Können wir die Resultate der Goldstandard–Diagnostik vollständig mit WGS und WTS erfassen und darüber hinaus zusätzliche Informationen generieren, die uns bezüglich Prognose und Therapieauswahl weiterhelfen?
- Wo sind die Vorteile der aktuellen Diagnostikmethoden im Vergleich zu den potentiell zukünftigen?
- Wie ist die Turn-Around-Zeit?
- Wie muss man die Kostenstruktur ansetzen (aktuell wäre das additiv), wie könnte sich das Ganze dann in Zukunft abbilden?
- Worauf sollten wir also in Zukunft unsere Forschungsfragen fokussieren?
Rekrutierung
Die Studie rekrutiert aktuell weiter. Eingebracht werden können Patienten, bei denen die Standard-Diagnostik noch Fragen offen ließ. Hier finden Sie den Anmeldebogen für die Studie sowie eine spezielle Einverständniserklärung (DSGVO und ISO konform) zum Download. Sofern Sie einen geeigneten Patienten für diese Studie ausgewählt haben, melden Sie diesen bitte per Email an torsten.haferlach@mll.com, um gemeinsam entscheiden zu können, ob WGS & WTS in der Konstellation hilfreich sein könnten.
Das neu zu entnehmende Untersuchungsmaterial (Blut, am ehesten aber wohl Knochenmark) wird mit den Goldstandard Analysen des MLL für die jeweilige Fragestellung untersucht (Kosten trägt das MLL). Parallel werden für diese Patienten zeitgleich das Genom und das Transkriptom untersucht (die Firma Illumina unterstützt bezüglich des Verbrauchsmaterials). Wichtig wäre hier, dass der Anteil der aberranten Zellpopulation im Blut oder Knochenmark >20% betragen sollte.
Rekrutierung: offen
Ergebnisse
Seit 09/2021 wurden 31 Patienten mit ungeklärtem Verdacht auf eine hämatologische Neoplasie in die Studie eingeschlossen. Es erfolgten sowohl die Standarddiagnostik entsprechend der WHO Kriterien als auch WGS und WTS Analysen. Im Vergleich zur Standarddiagnostik konnten WGTS Analysen bei 10/31 (32%) Patienten zusätzliche Informationen liefern. Meist handelte es sich um seltene SNVs (single nucleotide variants), die mit den Standard-Panels nicht abgedeckt werden, und CNVs (Kopienzahlveränderungen), die von zu geringer Größe sind, um mit bei der Chromosomenanalyse erfasst zu werden. Im Median wurden die WGTS Ergebnisse innerhalb von 21 Tagen nach Probenentnahme berichtet.
WGS identifizierte seltene SNVs
Zu den seltenen SNVs, die mittels WGS identifiziert wurden, gehörten auch Varianten mit Assoziation zur Diamond-Blackfan Anämie (RPL11) und zum VEXAS Syndrom (UBA1) sowie eine Variante unbestimmter Signifikanz mit möglichem Bezug zur Pelger-Huët Anomalie (LBR).
WGS klärte bereits bei der Chromosomenanalyse nachgewiesene SVs auf
Ein Patient mit Morbus Waldenström und ungewöhnlicher klinischer Präsentation wies eine Translokation t(14;19) auf, die typischerweise zu einem IGH::BCL3-Rearrangement führt. Mittels WGS wurde NECTIN2 anstelle von BCL3 als Partnergen der SV (strukturellen Veränderung) identifiziert – ein Gen, das bei T-Zell-Neoplasien in Translokationen involviert ist und bei DLBCL mit IGH rearrangiert beschrieben wurde.
WGTS führte zu neuen Erkenntnissen
Bei einem Patienten mit ungeklärter persistierender Zytopenie konnte mittels WGS eine Xq25-Deletion nachgewiesen werden, die das STAG2 Gen einschloss. So lieferten die Analysen den Nachweis einer klonalen Hämatopoese und die Diagnose CCUS konnte gestellt werden (siehe auch Case Reports).
Die WGTS Daten einer Patientin zeigten eine Duplikation dup(20q12), die zu einer TOP1::PLCG1-Fusion führte. Die Bedeutung dieser CNV ist unklar, die betroffenen Gene sind bei myeloischen und lymphatischen Neoplasien jedoch in andere SVs und SNVs involviert.
WGTS identifizierte Klone, die in vitro nicht proliferierten
WGTS Daten eines 26-jährigen Patienten zeigte eine SV der Chromosomen 11 und 17, die zu einer NUP98::BPTF-Fusion führte. Aufgrund der fehlenden Proliferation in vitro wurde der aberrante Klon bei der Chromosomenanalyse nicht erfasst. NUP98-Rearrangements treten vor allem bei Kindern mit AML und bei T-ALL auf. Speziell die Fusion NUP98::BPTF wurde bei einem Patienten mit akuter megakaryoblastischer Leukämie (AMKL) beschrieben.
WGTS detektierte therapeutisch relevante Veränderungen
Bei einem Patienten mit multiplem Myelom wurde im Rezidiv nach einer auf BCMA gerichteten CAR-T-Zelltherapie eine biallelische Deletion des Gens TNFRSF17 (BCMA) und eine stark reduzierte Expression von TNFRSF17 mittels WGTS nachgewiesen. Eine solche Inaktivierung des Targets und die daraus folgende Resistenz gegenüber einer Immuntherapie wurde bereits als irreversibel beschrieben (Da Vià M et al. 2021), sodass die gewonnene Information die weitere Therapie-Entscheidung relevant beeinflusst (siehe auch Case Reports).
Bei 32% der Patienten neue Informationen
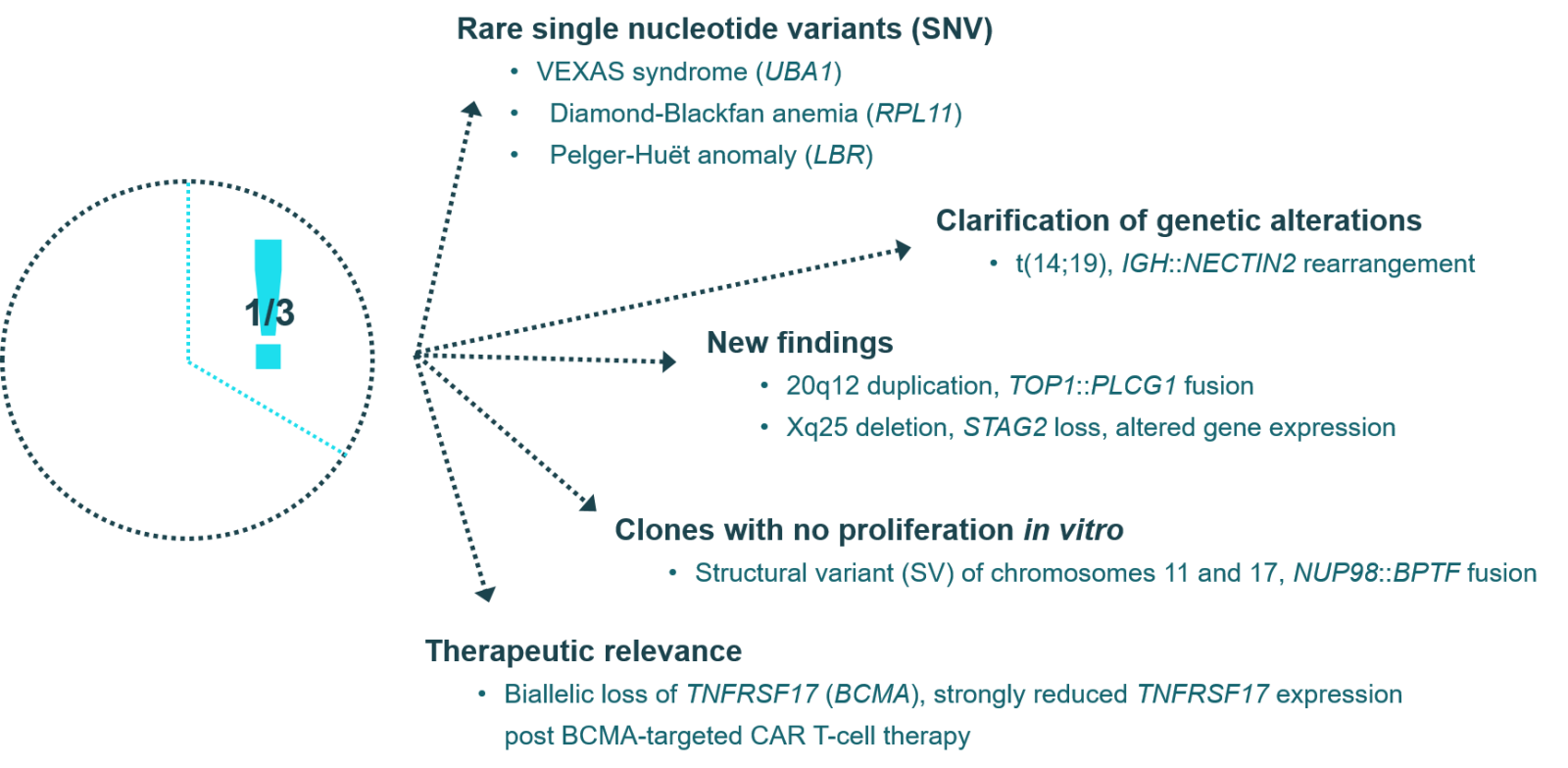
Der spannende Fall - SIRIUS Studie, durch WGTS Analysen gewonnene relevante Informationen.
Die ersten Ergebnisse der laufenden Studie zeigen, dass WGTS Analysen die Erkenntnisse der Standarddiagnostik in etwa 1/3 unklarer Fälle innerhalb von drei Wochen um wertvolle Informationen erweitern können.
Bei schwierigen Fällen ermöglicht eine enge Zusammenarbeit von Experten aus den Bereichen Hämatologie, Pathologie, Humangenetik und Bioinformatik die bestmögliche Nutzung dieser umfassenden Daten. In Tumorboards können so für die Patienten die zutreffendsten Diagnosen erzielt werden.